
 第1部目次
第1部目次

 前ページ
前ページ

 次ページ
次ページ
  第1部目次
第1部目次
  前ページ
前ページ
  次ページ
次ページ
|
1-2: 原子の発見 |


|
 「デモクリトスの原子論」 「デモクリトスの原子論」

 物質が最小の単位 物質が最小の単位
 すなわち 原子 (アトム) すなわち 原子 (アトム)
 から構成されている から構成されている
 という考え方は, という考え方は,
 古代ギリシャ哲学において 古代ギリシャ哲学において
 デモクリトス によって デモクリトス によって
 唱えられました. (紀元前 500 年頃). 唱えられました. (紀元前 500 年頃).
 「アトム」とは 「アトム」とは
 「分割できない」 「分割できない」
 という意味です. という意味です.
 デモクリトスは, デモクリトスは,
 この世は無限に広がる「空虚」と この世は無限に広がる「空虚」と
 その中を運動する「アトム」 その中を運動する「アトム」
 からできていると考えました. からできていると考えました.

 一方, アリストテレスは, 一方, アリストテレスは,
 世界は連続的な物質で 世界は連続的な物質で
 満たされている, 満たされている,
 と考えました. と考えました.
 古代から中世にかけて, 古代から中世にかけて,
 アリストテレス流の アリストテレス流の
 考え方が支配的でした. 考え方が支配的でした.

|
 「元素の存在」 「元素の存在」

 18世紀には 18世紀には
 実験化学が精密化されて 実験化学が精密化されて
 酸素や水素が発見され, 酸素や水素が発見され,
 アリストテレスなどの アリストテレスなどの
 4元素説 4元素説
 (世界は火, 水, 土, 空気 の (世界は火, 水, 土, 空気 の
 4つの元素から 4つの元素から
 できているという説) できているという説)
 が否定されるように が否定されるように
 なりました. なりました.
 ラボワジェ (フランス: 1743 - 94) ラボワジェ (フランス: 1743 - 94)
 は, は,
 通常の化学的手段では 通常の化学的手段では
 それ以上の異なる物質に それ以上の異なる物質に
 分けられない要素があり, 分けられない要素があり,
 これを これを
 元素 元素
 と定義しました(1789). と定義しました(1789).
 したがって, したがって,
 すべての物質はいくつかの すべての物質はいくつかの
 元素の組み合わせで 元素の組み合わせで
 できていると考えました. できていると考えました.

|
 「定比例の法則, 倍数比例の法則」 「定比例の法則, 倍数比例の法則」

 18 ~ 19世紀になると, 18 ~ 19世紀になると,
 実験事実に基づいた 実験事実に基づいた
 科学的な原子論 科学的な原子論
 が確立しました. が確立しました.

 まず, まず,
 「簡単な化合物には, 「簡単な化合物には,
 一定不変の量の成分元素が 一定不変の量の成分元素が
 含まれいる」 ことが明らかになりました. 含まれいる」 ことが明らかになりました.
 これを定比例の法則 これを定比例の法則
 といいます. といいます.
 例えば, 水は 例えば, 水は
 水素と 水素と
 酸素という 酸素という
 2種類の元素の化合物ですが, 2種類の元素の化合物ですが,
 どのような化合の方法をとっても, どのような化合の方法をとっても,
 できあがった水の中に含まれる できあがった水の中に含まれる
 水素と酸素の重量の比は 水素と酸素の重量の比は
 1:8 という一定の値です. 1:8 という一定の値です.

 さらに倍数比例の法則 さらに倍数比例の法則
 という重要な法則が明らかに という重要な法則が明らかに
 なりました. なりました.
 「2種類の元素が化合して, 「2種類の元素が化合して,
 2つ以上の異なる化合物を 2つ以上の異なる化合物を
 作る場合, 作る場合,
 一方の元素の一定質量に対する 一方の元素の一定質量に対する
 他方の元素の質量は 他方の元素の質量は
 各々の化合物の間で 各々の化合物の間で
 常に簡単な整数比 常に簡単な整数比
 になっている」, になっている」,
 という法則です. という法則です.
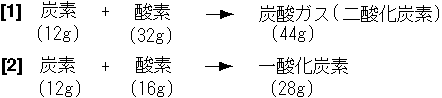
 例えば, 炭素と 例えば, 炭素と
 酸素を化合させて 酸素を化合させて
 炭酸ガス (二酸化炭素) と 炭酸ガス (二酸化炭素) と
 一酸化炭素を作る場合 一酸化炭素を作る場合
 を考えましょう. を考えましょう.
 12g の炭素をすべて 12g の炭素をすべて
 炭酸ガスにする場合 炭酸ガスにする場合
 32g の酸素が必要です. 32g の酸素が必要です.
 一方, 一方,
 12g の炭素がすべて 12g の炭素がすべて
 一酸化炭素になる場合には 一酸化炭素になる場合には
 16g の酸素が使われます. 16g の酸素が使われます.
 つまり, 12g の炭素にたいして つまり, 12g の炭素にたいして
 必要な酸素の質量の比は 必要な酸素の質量の比は
 32 : 16 = 2 : 1 です. 32 : 16 = 2 : 1 です.

|


|
 「ドルトンの原子論」 「ドルトンの原子論」

 上に述べた2つの法則は, 上に述べた2つの法則は,
 元素が 原子という基本単位 の 元素が 原子という基本単位 の
 集まりであると考えると, 集まりであると考えると,
 容易に理解できます. 容易に理解できます.
 これが ドルトン これが ドルトン
 (イギリス: 1766 - 1844) (イギリス: 1766 - 1844)
 による科学的な原子論です(1808). による科学的な原子論です(1808).

 下の式 のように, 下の式 のように,
 炭素と酸素が化合して 炭素と酸素が化合して
 炭酸ガス (二酸化炭素) と 炭酸ガス (二酸化炭素) と
 一酸化炭素ができる場合を 一酸化炭素ができる場合を
 例にとって説明しましょう. 例にとって説明しましょう.


|
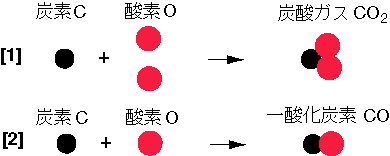
 下図 のように, 下図 のように,
 [1] の反応では [1] の反応では
 1 個の炭素原子 (C) が 1 個の炭素原子 (C) が
 2 個の酸素原子(O) と結合し, 2 個の酸素原子(O) と結合し,
 [2] の反応では [2] の反応では
 1 個の炭素原子 (C) が 1 個の炭素原子 (C) が
 1 個の酸素原子 (O) と結合 1 個の酸素原子 (O) と結合
 すると考えると, すると考えると,
 炭素原子の原子量 炭素原子の原子量
 (原子の質量) は 12, (原子の質量) は 12,
 酸素原子の原子量 酸素原子の原子量
 は 16 と考えられます. は 16 と考えられます.


 ドルトンはさ ドルトンはさ
 さまざまな化合物の中の さまざまな化合物の中の
 原子の組み合わせを, 原子の組み合わせを,
 ジグソーパズルを解くように ジグソーパズルを解くように
 明らかにしました. 明らかにしました.
 その結果,水は その結果,水は
 酸素原子1個と 酸素原子1個と
 水素原子2個が結合している 水素原子2個が結合している
 ものと考えられます. ものと考えられます.


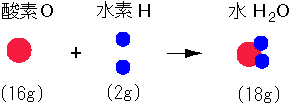
 したがって酸素の原子量を したがって酸素の原子量を
 16 とするならば, 16 とするならば,
 水素の原子量は 1 となります. 水素の原子量は 1 となります.

 このようにして このようにして
 物質を構成する 物質を構成する
 最も基本的な単位が 最も基本的な単位が
 原子 (アトム)であるという 原子 (アトム)であるという
 考え方が定着しました. 考え方が定着しました.

|
 「原子量」 「原子量」

 ドルトンの原子論で ドルトンの原子論で
 明らかになったように, 明らかになったように,
 水素原子の原子量を 水素原子の原子量を
 1 とすると, 1 とすると,
 炭素は約 12, 炭素は約 12,
 酸素は約 16 となり 酸素は約 16 となり
 比較的軽い元素の原子量は 比較的軽い元素の原子量は
 ほぼ整数に近くなりますが, ほぼ整数に近くなりますが,
 重い元素になると 重い元素になると
 整数からずれてきます. 整数からずれてきます.

 現在では,原子の質量は 現在では,原子の質量は
 原子質量単位 (u) 原子質量単位 (u)
 であらわされます. であらわされます.
 これは炭素を標準にし, これは炭素を標準にし,
 炭素の同位元素 (同位体) の 炭素の同位元素 (同位体) の
 中で 最も多く存在する 中で 最も多く存在する
 炭素12の質量を 12 u として, 炭素12の質量を 12 u として,
 ほかの元素の相対的な ほかの元素の相対的な
 質量を示すものが 質量を示すものが
 原子量です. 原子量です.
 つまり,炭素12の原子の つまり,炭素12の原子の
 原子量は 12 [u] です. 原子量は 12 [u] です.


 1 u = 1.6605402 x 10-27 kg.
1 u = 1.6605402 x 10-27 kg.

 自然界に存在する 自然界に存在する
 元素の中には 元素の中には
 質量の異なる 質量の異なる
 同位体 同位体
 が含まれていて, が含まれていて,
 その割合 (存在比) は その割合 (存在比) は
 元素によります. 元素によります.
 したがって, したがって,
 元素の原子量 は 元素の原子量 は
 各元素の同位体の 各元素の同位体の
 質量に 質量に
 同位体の存在比 同位体の存在比
 をかけて平均値を をかけて平均値を
 とったものになります. とったものになります.
 例えば, 炭素の 例えば, 炭素の
 原子量は 原子量は

 12×0.989+13.00×0.011=12.01 [u]
12×0.989+13.00×0.011=12.01 [u]

 となります. となります.
 そうすると,水素は 1.008 [u], そうすると,水素は 1.008 [u],
 ヘリウムは 4.003 [u], ヘリウムは 4.003 [u],
 酸素は 16.00 [u], 酸素は 16.00 [u],
 ナトリウムは 22.99 [u] ナトリウムは 22.99 [u]
 となります. となります.

|
 トップ
トップ
|
|
 第1部目次へ戻る
第1部目次へ戻る

 前ページへ戻る
前ページへ戻る

 次ページへ進む
次ページへ進む
|